Lectura 2:00 min
AstraZeneca reanuda los ensayos de su vacuna contra Covid-19 en Reino Unido
La empresa farmacéutica dijo que reanudará los ensayos clínicos en otros países cuando las respectivas autoridades lo autoricen, con el objetivo de "suministrar una vacuna de forma amplia, equitable y sin buscar beneficios durante esta pandemia".
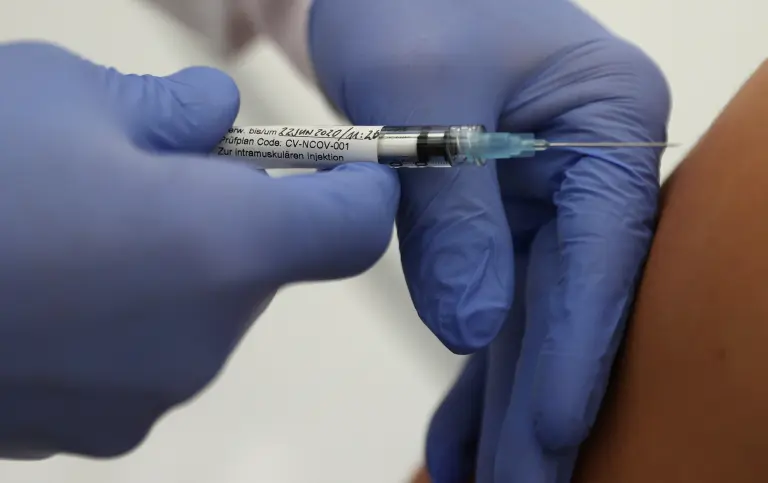
Foto: Reuters
El gigante farmacéutico AstraZeneca anunció el sábado 12 de septiembre la reanudación de los ensayos clínicos para lograr una vacuna contra Covid-19, que había interrumpido ante la enfermedad de un voluntario, tras obtener la autorización de las autoridades británicas.
Los ensayos clínicos para la vacuna AstraZeneca Oxford contra el coronavirus, AZD1222, se han reanudado en el Reino Unido tras recibir confirmación de la Autoridad de regulación sanitaria", informó la compañía.
AstraZeneca anunció el martes 8 de septiembre que había interrumpido "voluntariamente" las pruebas de la vacuna que está elaborando junto a la Universidad de Oxford después de detectar que uno de los voluntarios había desarrollado una enfermedad "inexplicada".
Un comité independiente examinó las medidas de seguridad de los ensayos, un paso que tanto la multinacional como la Organización Mundial de la Salud (OMS) calificaron de rutinario en estos casos.
El comité "ha concluido sus investigaciones y ha confirmado a la Autoridad que los ensayos son seguros", añadió AstraZeneca.
La vacuna de esta empresa es una de las nueve que se está ensayando en estos momentos en el mundo de forma masiva con seres humanos, lo que se conoce como Fase 3.
Los gobiernos de México y Argentina están a la espera de los resultados de estas pruebas para poder producir y distribuir esta vacuna en América Latina con el financiamiento de Fundación Slim.
En Estados Unidos AstraZeneca empezó el 31 de agosto a enrolar a 30,000 voluntarios, y la inoculación ya ha empezado con pequeños grupos en Brasil y otros países latinoamericanos.
La vacuna AZD1222 utiliza una versión más benigna del adenovirus que causa el resfriado común, pero modificado genéticamente para luchar contra la proteína que el Covid-19 utiliza para invadir las células humanas.
Al ser vacunado, el paciente empieza a producir esa proteína, lo que permite al sistema inmunitario atacar al coronavirus si éste penetra en el cuerpo.
AstraZeneca aseguró que mantiene los más altos estándares de seguridad, y que reanudará los ensayos clínicos en otros países cuando las respectivas autoridades lo autoricen, con el objetivo de "suministrar una vacuna de forma amplia, equitable y sin buscar beneficios durante esta pandemia".














